
#Thieme未来星计划荣誉推出神经病学专题,我们将与未来星计划的小伙伴们持续推荐解读与神经病学相关的论文与研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
刘梦真 | 首都医科大学
↓ 神经病学专题丨03
体位性低血压(OH)是指站立3分钟内收缩压(SBP)降低≥20mmHg或舒张压降低≥10mmHg。当我们站立时,重力作用会使大约700ml的血液流向下半身,使回心血量减少。通常,压力反射通过激活交感神经和收缩血管来代偿心脏前负荷的减少。当自主神经功能低下时,患者丧失直立体位时对血管收缩的调节功能就会造成直立性低血压。神经源性体位性低血压(nOH)可由神经退行性疾病引起,包括单纯自主神经功能衰竭和多系统萎缩,但在临床上更常见于糖尿病和帕金森病患者。
体位性低血压的常见症状是站立几秒钟后出现头晕目眩、视物模糊,以及颈部和肩部不适(呈“衣架”分布),可以通过坐下或躺下来缓解症状。这些症状的严重程度通常与血压的下降的幅度有关。
Semin Neurol 2020; 40(05): 515-522
DOI: 10.1055/s-0040-1713886
Review Article
Management of Orthostatic Hypotension, Postprandial Hypotension, and Supine Hypertension
体位性低血压、餐后低血压和卧位高血压的治疗
Cyndya A. Shibao, Italo Biaggioni
治疗
目前OH的治疗不以血压调整至正常水平为目的,而是着重减轻患者症状,降低晕厥和跌倒的风险。目前常用的治疗方案包括非药物治疗和药物治疗。
非药物治疗策略:首先要停用诱发或加重nOH的药物。如α 1受体阻滞剂、利尿剂、贝塔受体阻滞剂等。对于帕金森患者,建议减少多巴胺受体激动剂药物的剂量。其次OH的患者需要确保正常或更多的血容量,因此水的摄入可以增加到2-3升,当然还要取决于患者心脏和其他脏器的功能。可以通过物理治疗(反压力)来减少因重力作用导致的下肢血液聚集,如(弹力袜)。但对于帕金森和多系统萎缩的病人这可能会增加跌倒的风险。有研究表明,通过增加钠盐的摄入也可以增加中心血容量。除了以上方法,患者在3到4分钟内快速喝下500ml水也可以明显升高收缩压。
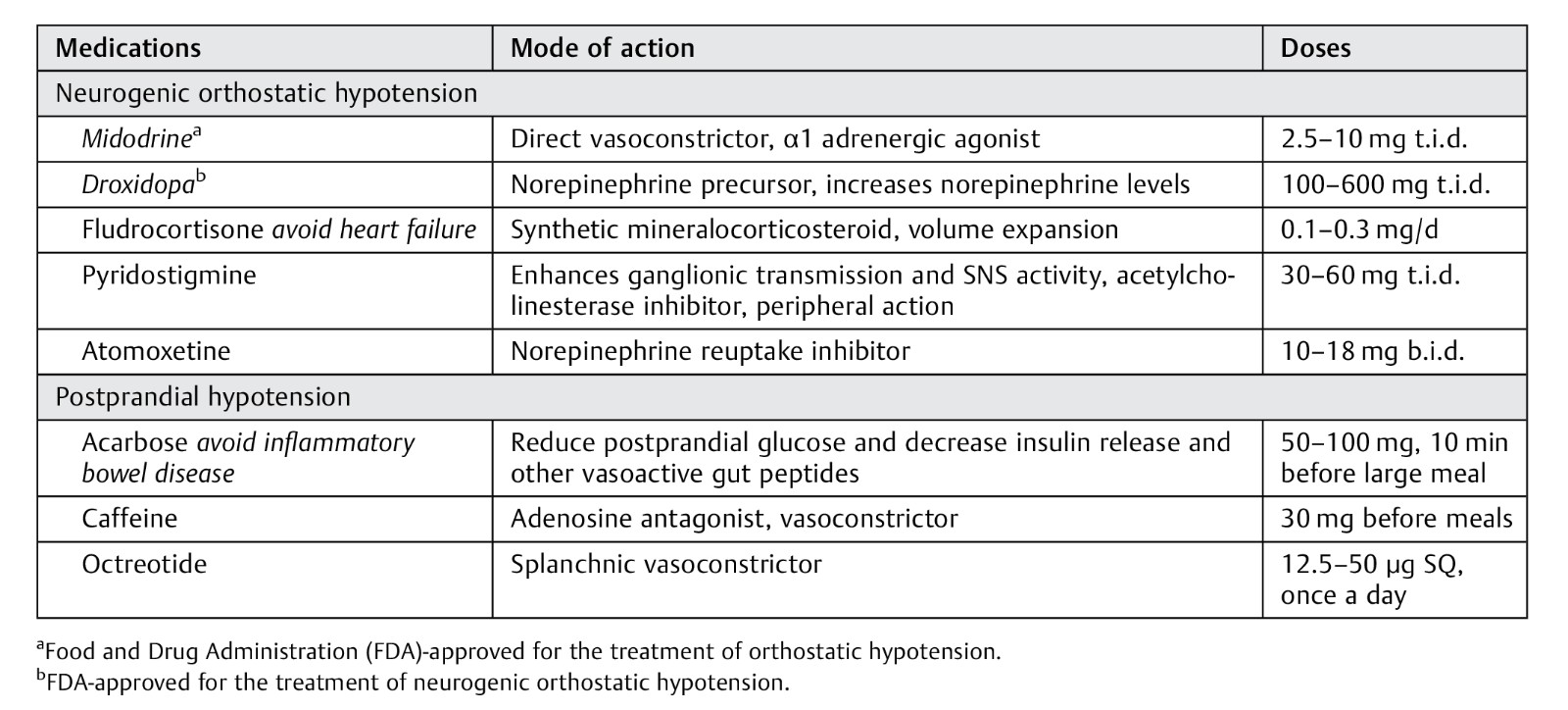
用于治疗体位性低血压和餐后低血压的常用药物
药物治疗治疗包括拟交感神经药物、增加血管内血容量的药等,下面会详细介绍。
拟交感神经药物
米多君通过外周α 1 肾上腺素受体激动剂收缩外周动脉和静脉血管。虽然它的半衰期仅有0.5小时,但它的活性代谢产物还可以接着发挥作用,因此可作用4小时左右。常见的不良作用包括头皮异常感觉(特别是发痒)、竖毛反射、仰卧位高血压和尿潴留等。对肝功能不全和急性肾衰竭的患者应避免使用米多君。
屈昔多巴是去甲肾上腺素前体,通过多巴脱羧酶代谢形成去甲肾上腺素。屈昔多巴推荐的初始剂量是100mg/次,每天3次,每2-3天可以调整剂量,直到最高剂量600mg/次。严重的nOH患者,能耐受每天增加100mg的快速增量方案。卧立位血压的加重是屈昔多巴的主要不良反应,因此可能更适合每天2次给药。
溴吡斯的明是一种胆碱酯酶抑制剂,它通过自主神经节突触后膜上的烟碱乙酰胆碱受体增加自主神经节的信号传递,因此它适用于交感神经功能尚存、病变程度较轻的患者。在一项nOH患者口服60mg溴吡斯的明的双盲/随机研究中发现,它可以在显著改善直立性症状的同时而不引起卧立位高血压。关于它治疗nOH的的治疗有待于进一步研究。
增加血管内血容量的药
氟氢可的松是一种具有盐皮质激素的合成类固醇,可增强肾小管对钠的重吸收,并促进钾和氢的置换。然而,氟氢可的松通过肾钠再吸收对血容量的影响仅持续几周。推荐的起始剂量0.1mg/天,最高剂量为0.3mg/天。约50%的患者在用药1周后可出现低钾的症状。因为它会加重仰卧位高血压(SH),对于不能耐受血容量增加的患者,如充血性心力衰竭、肾功能衰竭的患者不推荐使用该药。
餐后低血压(PPH)常发生于老年人,大约有超过90%的OH患者有餐后低血压,可能与老年人血压调节功能下降有关。PPH的定义为餐后(30分钟内收缩压下降超过20mmHg.研究发现,PPH的发生与姿势变化无关,并容易出现症状性低血压、晕厥和跌倒等症状。收缩压的降低幅度与饮食结构有关,特别是摄入大量碳水化合物。
阿卡波糖是治疗PPH首选药物。它一种-α葡萄糖苷酶抑制剂,能够通过可逆性结合肠道α-葡萄糖苷酶减少进食后葡萄糖的吸收。但长期使用阿卡波糖可能会增加胃肠胀气和腹泄的发生率。推荐以小剂量(25mg)开始治疗,并逐渐增加至100mg,每天1到2次,直到症状缓解。不推荐糖尿病酮症酸中毒、肝硬化、炎症性肠病、溃疡性结肠炎、肠梗阻或任何可能破坏消化或吸收的慢性肠道疾病的患者使用。咖啡因在饭前30分钟服用,可有效减轻PPH。此外,奥曲肽对中毒PPH患者也有帮助,其缺点是皮下给药、腹痛、恶心、呕吐等副作用。
卧位高血压(SH)是仰卧位时,收缩压>=150mmHg或舒张压>=90mmHg。据估计,约有50%-60%的nOH患者伴有仰卧位高血压。通常血压在坐位时测量,因此临床中容易忽略。导致卧位高血压的因素很多,如用于治疗OH的药物可能会导致持续性卧位高血压,特别是像氢化可的松这样半衰期长的药物;许多原发性高血压的患者,因为自主神经功能的紊乱也可能会使血压恶化。
SH不仅限制对患者的nOH的治疗,同时也可能增加靶器官的损害。24小时动态血压监测仪可用于评估夜间或清晨血压的下降情况。
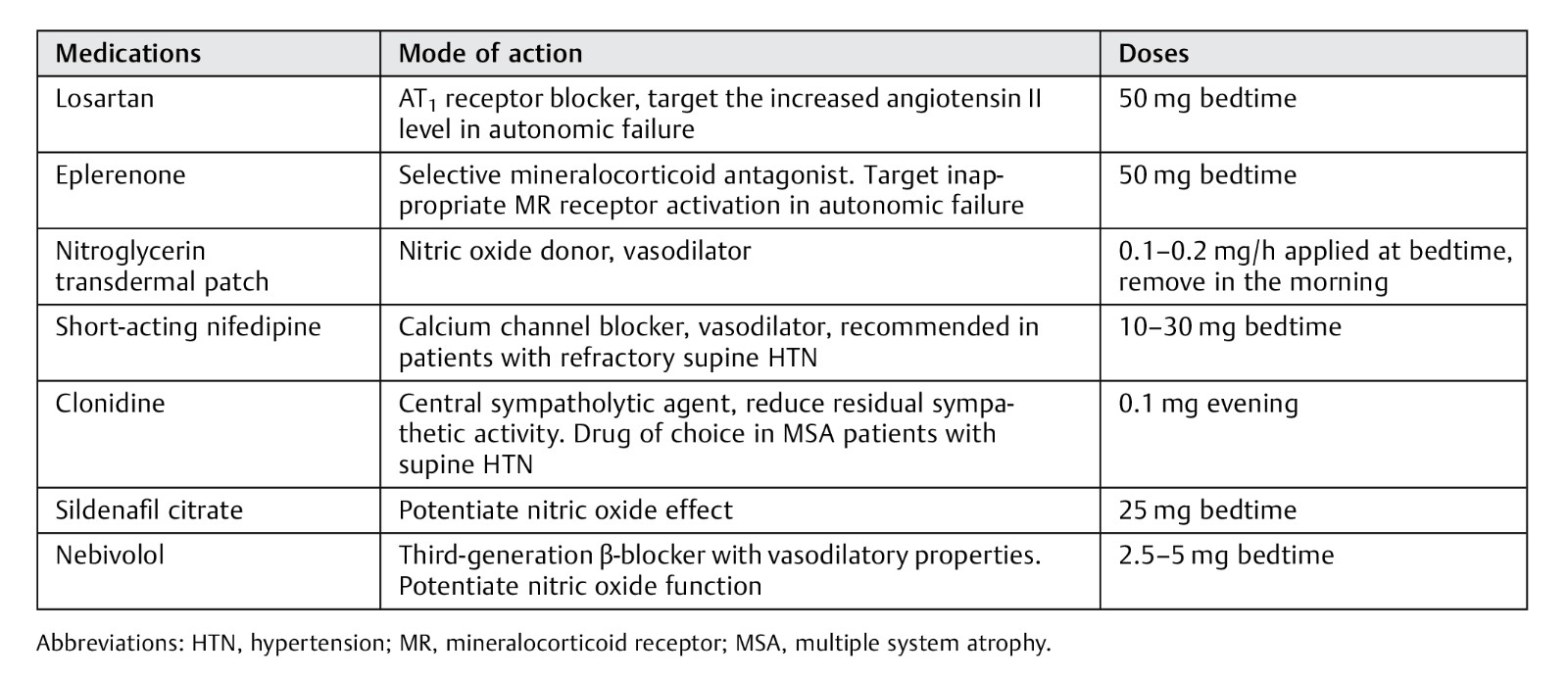
卧位高血压治疗药物
对于卧位高血压的治疗,如果患者出现了靶器官的损害(如左心室肥大、肾功能损害)建议开始治疗。非药物治疗:最有效的方法是避免卧位,尤其是在使用升压药治疗OH的数小时内。其他包括睡前吃甜食或将床头抬高。药物治疗包括肾素血管紧张素AT1受体拮抗剂氯沙坦可降低夜间血压,给药后6小时可使血压下降32mmHg。此外醛固酮受体拮抗剂依普利酮同样有效。增加一氧化氮的枸橼酸西地那非、交感神经抑制剂可乐定都证明有效,例如,在多系统萎缩患者中,可乐定在给药后6小时内可使血压降低约26mmhg。
目前由于治疗选择很少,nOH 的治疗很困难,过去 20 年中只有两种 FDA 批准的药物(米多君和屈昔多巴)。小型临床研究表明,氟氢可的松、吡啶斯的明可用于治疗nOH。卧位高血压和餐后低血压等合并症使 nOH 治疗复杂化;阿卡波糖是唯一明确针对餐后低血压的可用药物。nOH合并有卧位高血压的患者需要白天联合升压药,夜间联合短效降压药治疗。其中,奈必洛尔、氯沙坦、依普利酮对控制夜间卧位高血压有效。大多数患者中,可以在不加重日间 OH 的情况下控制卧位高血压。大多数 nOH 患者可以通过非药物联合药物治疗来缓解症状。治疗nOH任重而道远。
阅读本刊更多论文,请点击这里。
