

Synthesis
Reviews and Full Papers in Chemical Synthesis
影响因子 2019:2.675
BY
谢伟彬 南开大学 | 推荐&解读

A. Uttry, M. van Gemmeren
背景
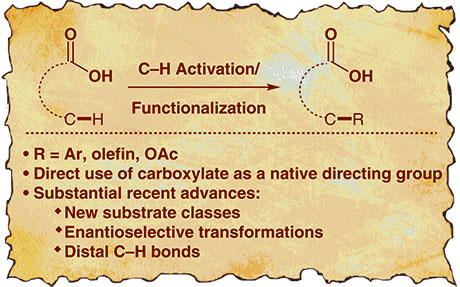
羧酸在有机化学中有着重要的地位。它们便宜易得,来源丰富,因此在有机化学中常用来起始原料、合成中间体以及产物。在化工上,羧酸常用来溶剂、农药化学品以及药物。羧酸可以通过醇或烷烃的氧化而容易获得,并且可以进一步转化为其他有用的官能团。
除了脱羧方法外,人们还非常关注将羧酸部分用作C–H活化/官能化反应的直接导向基团。此类反应非常有趣,因为它们无需提前功能化即可快速进入复合物分子。重要的是,C-H活化也在天然产物合成中有着越来越多的应用。对于芳族羧酸,羧酸官能团可以在多种情况下用作导向基团已得到验证。但是,对于羧酸对脂肪族C-H键的定向活化作用,仅报道了有限数量的反应。这种类型的C–H活化已被证明具有挑战性,大概是由于活化熵高,以及过渡金属与芳族π系统之间缺乏预配位。
挑战
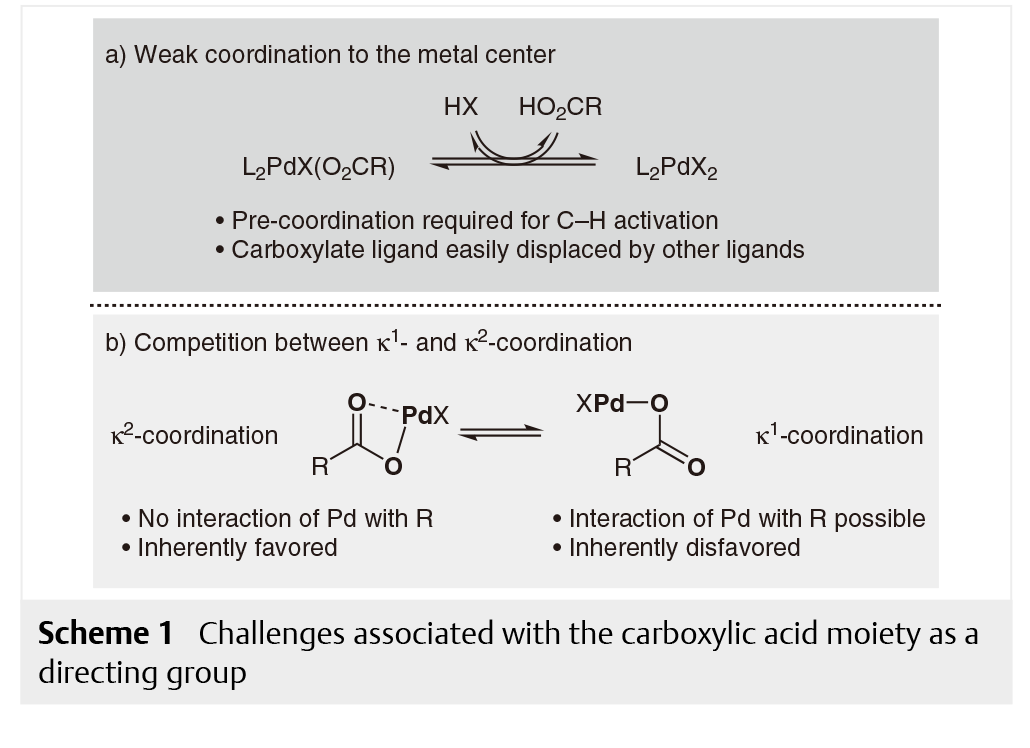
通常,脂肪族化合物C-H活化过程面临着热力学稳定性和C-H键的非极性的挑战,然而在这一过程中过渡金属插入C-H键成为关键步骤。为了实现C–H活化,过渡金属必须紧邻各自的C–H键。这通常使用导向基团来实现,其中预配位使过渡金属靠近目标C–H键。反应发生通常需要通过络合诱导的邻近效应来加速。此外,这种预配位还决定了C-H活化过程的区域选择性。尽管已经证明该方法非常成功,但是使用游离羧酸部分作为直接导向基团仍然有无与伦比的吸引力。与包含强结合亚基(如氮基杂环,卡宾或膦)的配体和底物相比,羧酸与过渡金属配位较弱。因此,该羧酸可以容易地被反应混合物中存在的其他阴离子替代(方案[1,a])。这种类型的平衡减少了系统中反应物的数量,因此不利于整体反应效率。
当与过渡金属催化剂结合时,羧酸可以以两种不同的配位方式与金属中心结合(方案[1,b])。在κ2配位模式下,金属与羧酸盐的两个氧原子配位,而在κ1配位模式下,只有一个氧原子的单孤对与金属配位。其中,只有κ1配位的复合物可以在金属中心与要激活的C-H键之间有着适当的构象。
总结
尽管与具有更强导向基团的反应相比,脂肪族羧酸的C–H活化作用仍不发达。近年来,人们已开始着手研究将羧酸官能团用作直接导向基团。据报道,通过采用特定配体和反应条件可以解决羧酸的弱导向基团的问题。目前这些方法已经扩展到广泛的亲电试剂中,而这些亲电试剂与强导向基团一起使用,似乎能够得到较好的结果。
但是, C–H的激活步骤仍然具有很高的挑战性。我们应该注意的是,想办法理解机理以及关键因素会对机理会产生怎样的影响,这些还尚未得知。此类反应的机理研究极具挑战性,原因在于:(a)典型反应混合物的多相性;(b)银盐的存在与C–H键的活化有着什么样的关联;(c)单体和高聚合的钯配合物之间的平衡,(d)催化剂与底物之间以及催化剂与配体之间的各种配位方式;(e)高极性溶剂可能与羧酸之间存在氢键,而氢键可能会对反应结果有着一定的影响。
然而,对机理的了解将在未来的发展中有着指导性的作用,例如将这些转变扩展到无偏向底物中的γ-C-H键或β-亚甲基C-H键。解决这些底物类别可能需要开发新的配体和反应条件。另外,许多当前方案使用当量的银盐和特定的溶剂,这对反应的可扩展性构成了很大的障碍。因此,对该反应的研究还应该深入进行。
