
Outcome of Emergency Pulmonary Lobectomy under ECMO Support in Patients with COVID-19
新冠肺炎患者ECMO支持下急诊肺叶切除术的疗效
Almeida et al.
**中文内容仅供参考,一切以英文原文为准。
2020年2月,严重急性呼吸综合征冠状病毒2型(SARS-CoV2)和由此引发的2019冠状病毒病(新冠肺炎)大流行袭击了欧洲,并带来了前所未有数量的急性呼吸道症状患者。这些患者中有相当一部分出现了急性呼吸窘迫综合征(ARDS),需要加强护理并最终进行机械通气。尽管进行了最大程度的强化治疗和广泛的医疗管理,但一些患者有呼吸机支持障碍,并因此考虑应用体外真膜氧合(ECMO)。虽然ECMO在非COVID-19 ARDS中的作用已得到很好的验证,但并没有在COVID-19引起的ARDS中使用ECMO的经验。同时,几项研究有效证明,ECMO可作为选定的与COVID-19肺炎相关的ARDS危重症患者的抢救疗法。虽然已确定对符合条件的新冠肺炎患者应用ECMO以克服呼吸机支持的失败,关于这些患者的胸部手术干预的结果,只有有限的数据。随着越来越多的新冠肺炎患者接受ECMO支持,可以假设,在这种困境下,胸外科医生将越来越多地面临提供手术治疗的任务。到目前为止,几个病例系列已见报道,主要涉及对呼吸急促、胸腔积脓和血胸等疾病的小手术干预。相比之下,研究者们并不了解对新冠肺炎患者应用ECMO进行解剖肺切除的结果。为了填补这一空白,研究者们决定报告使用ECMO时对新冠肺炎患者进行大型胸部手术的经验。本研究的目的是分析重症新冠肺炎所致急性呼吸衰竭患者在ECMO支持下进行非选择性肺叶切除术和全肺切除术的适应症和结果。
患者和方法
伦理声明
当地伦理委员会批准了这项研究(Az.22-190),由于采用了回顾性研究设计,因此无需获得个人书面同意。此外,在本机构,所有新冠肺炎感染的住院患者,或者更确切地说,他们的法定代表人,通常同意以匿名形式科学地使用他们的病例史来研究新冠肺炎泛流行。该研究符合《赫尔辛基宣言》。
在一项前瞻性收集数据库的回顾性研究中,研究者们分析了在德国一所大学医院接受ECMO支持下紧急解剖肺切除的新冠肺炎患者的所有病例。卡尔·古斯塔夫·卡鲁斯大学医院(德国德累斯顿)是萨克森州南部和东部(包括州府德累斯顿在内)约200万人口的唯一ECMO中心。在第三波疫情期间,萨克森州是德国疫情最严重的地区之一。
ECMO配置
在本研究中,需要ECMO来支持新冠肺炎感染引起的呼吸衰竭和ARDS患者的肺功能。由于不需要心循环支持,所有病例均采用双位点配置的静脉-静脉ECMO(vv ECMO)和外周血管通路。双位点vv ECMO优于单位点vv ECM,因为它允许更高的体外血流量,从而产生更好的氧合。ECMO是在Maquet心脏辅助系统(GETINGE AB,Göteborg,Sweden)的帮助下建立的。各种尺寸和插入长度的HLS套管(GETINGE AB,Göteborg,Sweden)用于单个外周套管。Seldinger技术中超声引导下的经皮插管是在胸腔切开术前在重症监护室(ICU)或手术室完成的。通常,在右颈内静脉和右股静脉进行插管,并将插管置于上下腔静脉。经食道超声心动图用于协助套管的最佳放置,并在手术期间监测心脏功能。经皮插管均是由麻醉师和护士组成的专业团队(ECMO团队)进行。
抗凝治疗
由于严重的新冠肺炎与肺动脉栓塞风险显著增加有关,所有患者在ECMO之前就已经接受了使用普通肝素的全身抗凝治疗。放置ECMO后,继续抗凝,目标活化部分凝血活酶时间(aPTT)在60至70秒之间。在术后即刻,将aPTT调整在50至60秒之间,以降低术后大出血的风险。
肺叶切除术/肺切除术的适应症
在一次多学科共识会议上,来自麻醉学、重症医学、胸外科和ECMO专家的与会者讨论了肺叶切除术的可能指标,并就以下几点达成一致。
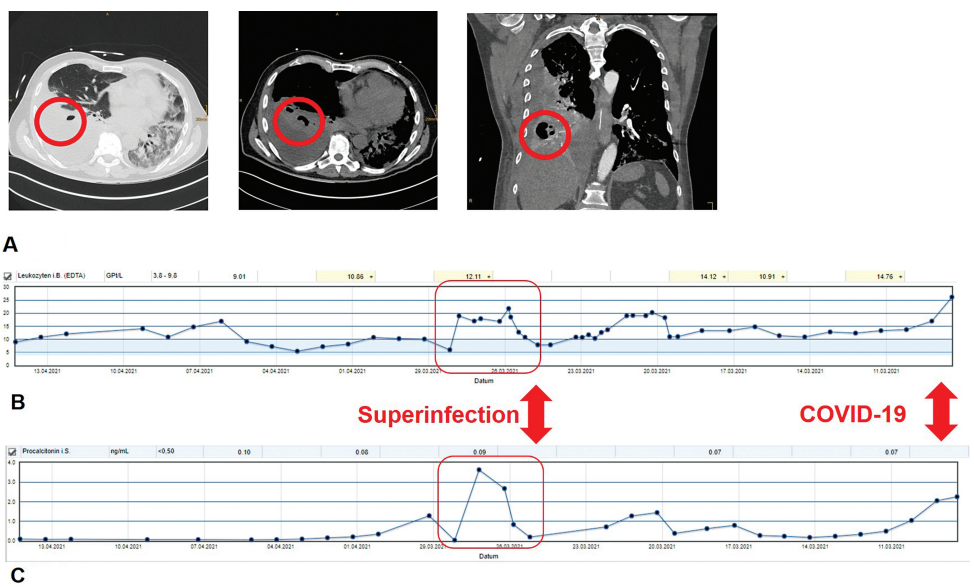
图1. 第二次出现细菌重叠感染。细菌重叠感染导致局部肺脓肿形成,伴有胸膜脓胸(A)和二次感染败血症,白细胞计数(B;时间线从右到左)和降钙素原(C;时间线由右向左)出现明显的新升高。
手术指征为细菌继发感染伴局部脓肿形成,以及在采用所有非手术医学和介入治疗后仍持续的脓毒症(►图1)。只有当所有非手术和介入手段都失败时,才考虑手术。介入治疗包括所有形式的内镜或图像引导干预,如经皮脓肿腔、胸膜腔或积液引流。细菌重叠感染被定义为在早期严重急性呼吸系统综合征冠状病毒2型感染之后或之上的第二次细菌感染。作为诊断的先决条件,细菌重叠感染必须通过支气管镜检查中获得的微生物样本来确认(►表1)。两肺弥漫性感染性病变和多发性脓肿因不适合通过手术治疗,因此被排除为手术治疗的指征。
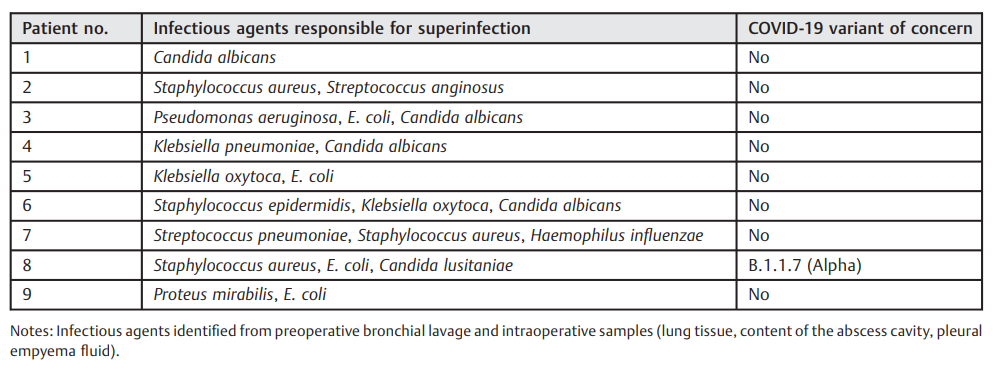
表1. 每位患者的微生物学结果
此外,脓肿腔内的肺出血或局部脓肿形成的大量支气管内出血被视为肺切除的指征。由于在急性情况下无法评估功能可操作性,COVID-19前良好的条件和性能状态是患者适合手术的强制性条件
操作技术
该系列仅包括肺叶切除术和全肺切除术等解剖性肺切除病例。所有程序都是在vv ECMO支持下进行的。在建立高流量体外循环(至少5 L/min)后,将患者置于侧卧位进行开胸手术。使用了标准的手术设备和商业缝合装置。由于所有患者都使用ECMO并接受了相关的抗凝治疗,导致出血趋势增加。因此,肺切除术后常规用纱布条填塞胸腔。患者在ICU病情稳定后,在初次手术后约48小时进行胸廓再切开术。如果出血情况得到控制,则取出包装材料,并最终闭合胸腔。在持续出血扩散的情况下,用纱布条重新包装,48小时后再次安排第三次手术。支气管残端的加固仅在最后一次胸廓再次切开时进行,以防止供体部位出血以及包装材料对皮瓣的损伤。全肺切除术后,支气管残端常规覆盖一个大而有活力的肌肉瓣。在肺叶切除术的情况下,加强支气管残端的决定是基于术中发现的肺部破坏和胸膜积脓的程度。
手术室团队安全
关于团队安全,在ICU和手术室中个人防护装备(PPE)都均常规使用(►图2)。所有手术都由同一团队执行,每个团队成员都收到了关于正确使用PPE的详细说明。在所有手术过程中,均常规使用耐流体长袍、手套、FFP3口罩和带面罩的头盔以及空气输送装置(3M Versaflo M系列,3M,Bracknell,UK)。
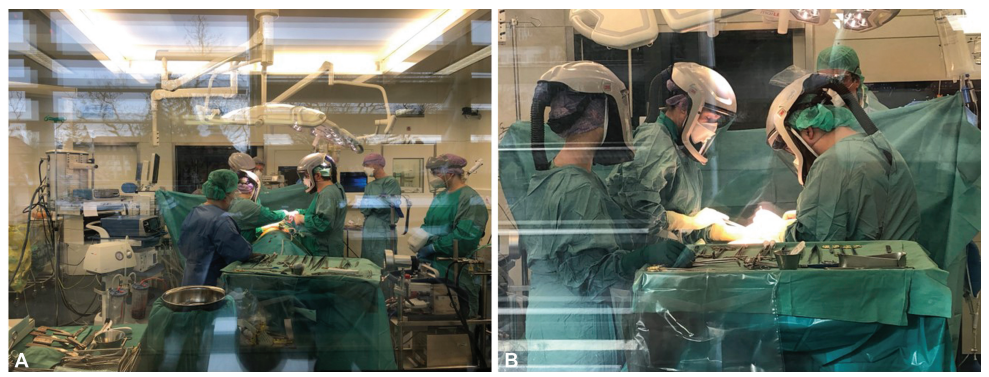
图2.(A、B)手术室团队安全。在所有手术过程中,常规使用个人防护装备,如防流体长袍、手套、FFP3口罩和带面罩的头盔以及空气输送装置。
术后护理
术后,所有患者均在麻醉ICU接受治疗,并接受了全方位的败血症治疗,包括血液动力学监测和管理、抗生素治疗、肾衰竭时的血液过滤和不同的机械通气。气管切开术在术后早期进行。ECMO治疗由专门的ECMO团队进行常规管理和监测。每天进行强化理疗。
ECMO切断
一旦观察到肺功能充分恢复,二氧化碳清除率和氧合得到改善,就尝试切断体外呼吸支持。ECMO血流和吹扫气逐渐回归使用。体外血流量逐渐降至约1.5 L/min,最终关闭吹扫气流。如果血气保持稳定,没有出现呼吸问题,则决定拆除该系统。短暂停止肝素治疗,并检测aPTT、血小板计数和国际标准化比率。如果无人反对,该系统最终被移除。除颤始终由ECMO团队的专家进行。由于血管通路仅为外周、经皮和静脉通路,因此在ICU进行拔管,并手动按压通路部位。血管外科干预并不在常规计划中。
统计分析
研究者们收集了以下关于初始表现、治疗、临床过程和结果的数据:人口特征、先前存在的合并症、首次COVID检测结果呈阳性的日期、住院和入住ICU的日期、新冠肺炎感染相关并发症(如气胸)、ECMO应用日期、手术日期、手术程序、术后过程以及结果。使用统一的数据收集表收集所有数据。使用R语言和环境进行统计分析(R统计计算基金会,奥地利维也纳;http://www.R-project.org)。
数据可用性声明
所有相关数据均收录在文中。
结果
在研究期间(2020年4月1日至2021年4月30日),德累斯顿(德国萨克森州)共有26645例新冠肺炎确诊病例。其中2327例入住德累斯顿市内的多家医院。实际上,他们中的大多数人在德累斯顿大学医院接受住院治疗(2327例中的1474例;63.34%)(►图3)。在这1474名患者中,343人(23.27%)需要在麻醉学ICU接受重症监护,其中123人最终需要vv ECMO治疗进行通气支持。最终,其中9人在接受ECMO时接受了肺叶切除术或全肺切除术(►图3)。

图3. 患者流程图。研究期间,共有1474名新冠肺炎患者住院治疗。其中,343人住进了重症监护室,123人需要ECMO治疗,9人最终在接受ECMO治疗时因肺脓肿接受了肺叶切除术。新冠肺炎,2019冠状病毒病;体外膜肺氧合;重症监护室,重症监护室。
外科病人的特点
手术组共包括9名确诊感染新冠肺炎的患者(2名女性和7名男性)(►表2)。中位年龄为61岁(四分位数1 55,四分位数2 65,四分位间距10岁),几乎没有预先存在的合并症(合并症的平均Charlson评分为0.2)。麻醉团队在手术时对患者进行评估后,美国麻醉师协会的平均分为4.22。所有患者均在vv ECMO下进行股颈静脉构型。手术前平均ECMO天数为6±7.07天,手术前平均ICU天数为15.4±5.17天,首次新冠肺炎检测呈阳性与手术之间的平均间隔为21.9天(范围9-37天)(►表2)。
手术时,所有患者都患有严重败血症(九分之九)和ARDS伴呼吸衰竭(九分之九)。其他症状包括需要血液透析的急性肾功能衰竭(九分之五)、CT肺动脉造影证实的肺动脉栓塞(九分之四)、使用ECMO时的自发性肺内出血(九分之二)、肺气肿(九分之二)、纵隔充血(九分之一)和胸膜积脓(九分之五)(►表2)。胸膜感染的RAPID平均评分为3.44±1.26。
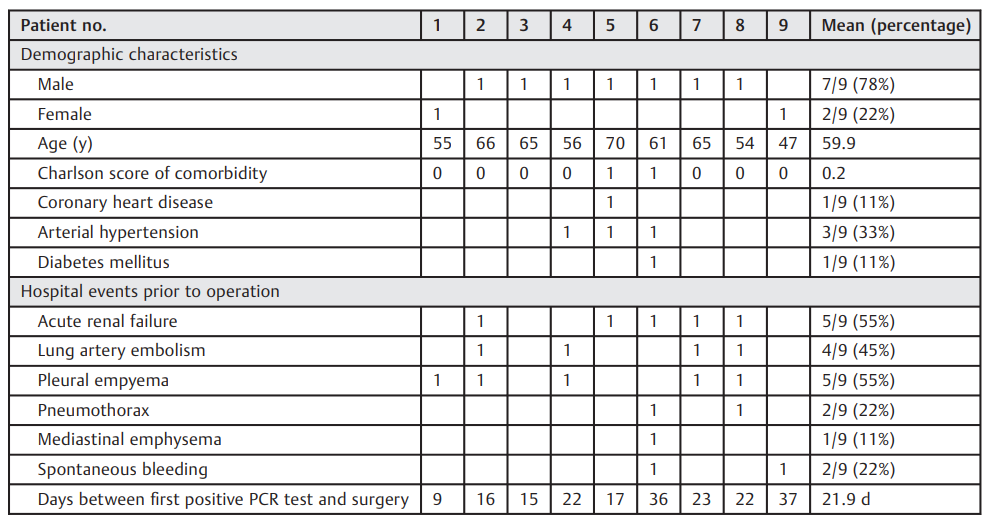
表2. 患者特征
手术适应症、手术程序和结果
手术适应症为细菌重叠感染伴局部肺脓肿形成和进行性脓毒性休克(九分之七)(►图1)或大量肺出血(九分之二)进入脓肿腔。手术程序为肺叶切除术(8例)和全肺切除术(1例)(►表3)。所有病例都常规用纱布条填塞胸腔。有7名患者进行了计划的胸廓再切开术,其中2名患者在计划的再次手术时间前死于重症监护室的难治性感染性休克。在7名住院患者中,包括初次手术和所有计划的再次开胸手术在内的平均开胸次数为3(范围2-5)。在这七名患者中,又有两名死于治疗性难治性感染性休克。另一名患者出现基底节大面积梗死,在与家人协商后停止治疗。住院总死亡率为九分之五(►表3)。在九名患者中,有四名成功脱离ECMO。整个组的平均ECMO总天数为10.3±6.2天,平均ICU总天数为27.7±9.9天,平均住院时间为28.7±8.8天。所有四名成功脱离ECMO的患者最终都出院到康复机构,在研究期结束时均仍存活。
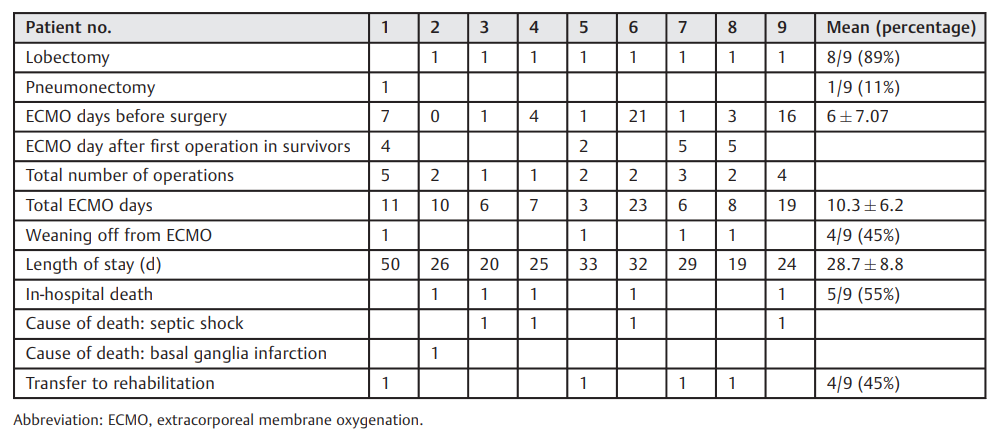
表3. 手术程序和结果
讨论
据研究者们所知,新冠肺炎患者在ECMO支持下进行肺叶切除术和肺切除术的第一个实质性病例系列之一已被报告。到目前为止,关于新冠肺炎患者非选择性解剖肺切除的单一病例报告仅有少数发表,除了一例外,均没有应用ECMO。总的来说,关于正在进行ECMO治疗的新冠肺炎患者的胸部手术的文献相当少。大多数情况下,研究仅报告简单的干预措施,如气管切开术、胸管插入术和电视胸腔镜治疗血胸或胸腔积脓。因此,研究者们想分享在正在进行的ECMO治疗下对新冠肺炎患者进行非选择性胸部大手术的经验。
德累斯顿ECMO中心多年来一直是东德主要的ECMO提供商,在非COVID-19病例中应用ECMO治疗ARDS方面拥有丰富的经验。2020年3月,当严重急性呼吸系统综合征冠状病毒2型大流行首次在萨克森州和东德出现时,几乎没有在新冠肺炎引起的ARDS患者中使用过ECMO。然而,新冠肺炎ARDS和腹壁难治性呼吸衰竭患者的ECMO治疗最快于2020年3和4月在德累斯顿大学医院开始。尽管当时缺乏证据,但世界各地都认为,严重急性呼吸系统综合征冠状病毒2型流行初期的特殊情况证明了使用ECMO的合理性。与此同时,单中心经验以及大型国家甚至超国家调查研究已见报道。最近公布的数据清楚地证明了ECMO可用于COVID-19诱导的ARDS。
在大流行期间,随着ECMO使用率的提高,据估计胸外科医生迟早会面临在使用ECMO时为新冠肺炎患者提供手术的任务。在这件事上,关键的是区分新冠肺炎患者在使用ECMO时的ECMO相关并发症的小手术干预和大胸部手术,如解剖肺切除。在过去几年中,经验丰富的ECMO中心报告了非COVID-19患者因血胸或胸膜脓胸等ECMO相关并发症而进行主要次要胸部手术干预的病例系列。新冠肺炎患者可能出现类似的ECMO相关并发症。与此同时,一些机构业已发表了关于这些并发症的手术管理的报告。另一方面,显然大型胸部手术在新冠肺炎的一线治疗中没有发挥任何作用,而是保守用于严重急性呼吸系统综合征冠状病毒2型感染的后期影响,如大量肺出血或细菌重叠感染。
就病毒性肺炎而言,自1918-1919年“西班牙流感”流行以来,细菌重叠感染是一种众所周知的现象。就严重急性呼吸系统综合征冠状病毒2型感染而言,既存在合并感染,也有细菌重叠感染。首次聚合酶链式反应检测呈阳性时的细菌合并感染非常常见(7.1-9.1%),必须在最初的抗菌治疗中解决以防止并发症。然而,细菌重叠感染通常发生在新冠肺炎后期。几项研究表明,细菌重叠感染率在16%至41%之间。在新冠肺炎患者中,接受重症监护的患者细菌重叠感染更为常见。埃彭多夫大学医院(德国汉堡)的一项分析发现,2020年3月至11月期间,在ICU接受机械通气的102名新冠肺炎患者中,有74人(72.5%)出现细菌重叠感染。
研究的所有患者都存在微生物证实的细菌重叠感染。这些标本是通过支气管镜从深呼吸道常规性获取的。计算机断层扫描显示细菌重叠感染导致肺脓肿形成和胸膜脓胸。在COVID19的第一个时期存活下来的新冠肺炎患者中, 细菌重叠感染和肺脓肿形成的发生构成了危险的第二次打击,最终可能导致新的败血症和感染性休克,并导致极高的死亡率(►图2)。研究团队先前关于感染性肺脓肿手术管理的工作清楚地表明,在严重败血症和败血症并发症发作之前及时进行手术干预是有益的。对于ECMO患者也是如此。因此,研究者们认为,通过切除受影响的肺叶来控制感染源将有利于克服突发情况。
研究者们将手术指征限制在局限性肺脓肿形成的病例,因为弥漫性病变通常不能通过手术干预来改善。在所有非手术治疗失败后,对受影响的肺进行肺叶切除术甚至全肺切除术被视为挽救患者生命的最后手段。考虑对ECMO患者进行解剖性肺切除的绝对先决条件是,术后脱离ECMO并不因肺切除的程度而变得困难甚至不可能。此外,必须考虑到,与非COVID-19患者相比,他们切除后剩余的肺也因SARS-CoV2感染的影响而严重受损。因此,研究者们只纳入了新冠肺炎疫情前表现良好且没有严重合并症的患者。
本研究方法在九分之四的患者中取得了成功。在第五例患者中,由于与肺叶切除术无关的原因停止了治疗,因此,该病例不应被视为细菌重叠感染引起的肺脓肿手术治疗的实际失败。ECMO的术中管理没有问题。包括计划的胸廓再切开术,研究者们对9名患者进行了20次手术,在插管位置、ECMO流量或气体交换方面没有遇到任何技术问题或任何困难。胸廓填塞和计划性胸廓再切开术成功地处理了出血增加的趋势。术后,研究者们没有遇到出血性休克,也不需要大量输血。
与此同时,关于新冠肺炎患者ECMO结果的几项研究已经发表。在这方面,单一机构的经验往往比多中心研究更有利。选定的单中心报告的死亡率为38%(16名患者中有6名)于柏林Charité医院(德国)、22%(9名)于苏黎世大学医院(瑞士)和仅10%(30名)于纽约大学朗格尼健康中心(美国纽约)。另一方面,美国最近的一项多机构分析显示,死亡率为50%(100例中有50例)。ECMOVIBER研究的范围包括西班牙和葡萄牙24个中心的338名接受ECMO治疗的新冠肺炎患者,结果显示死亡率为49%。包括德国所有医院的全国分析显示,vv-ECMO患者的死亡率为65.9%(3875例中有2552例)。
尽管这些研究的所有参与者都接受了新冠肺炎的ECMO治疗,但他们中没有一人在接受ECMO时接受了大型胸部手术,更不用说解剖肺切除了。因此,研究者们认为结果与目前的经验非常一致。在本系列中,非选择性肺叶切除术/全肺切除术并没有导致死亡率升高。相反,它有助于在没有手术干预的情况下实现新冠肺炎ECMO患者的预期结果。研究者们本以为结果会更糟。
局限
主要的局限性是,本研究仅为一个研究人群有限的单中心研究。仍需要一个多机构的研究项目来获得更多的证据。另一方面,这是第一个报道新冠肺炎患者在使用ECMO时进行肺叶切除术/肺切除术的实质性病例系列。因此,研究者们认为本结论对关于在严重急性呼吸系统综合征冠状病毒2型感染情况下使用ECMO的科学争议做出了重要贡献。
结论
总之,ECMO治疗下的肺叶切除术为新冠肺炎细菌重叠感染和局部肺脓肿患者的成功手术治疗开辟了一个前景。
评价
该论文是一项单中心研究,旨在分析重症新冠肺炎所致急性呼吸衰竭患者在ECMO支持下进行肺叶切除术的结果。研究发现,满足条件的九个患者(中位年龄61岁,四分位间距10岁)中有四例成功脱离ECMO。住院死亡率为九分之五。平均ECMO总天数为10.3±6.2天,平均ICU总天数为27.7±9.9天。平均住院时间为28.7±8.8天。令人欣喜的是,非选择性肺叶切除术/全肺切除术并没有导致死亡率升高。相反,它是在没有其它手术干预的情况下实现新冠肺炎ECMO患者的预期结果的有效手段。ECMO支持下的急诊手术为新冠肺炎细菌重叠感染和局部肺脓肿患者的手术源头控制开辟了前景。但值得改进的是,此研究仅为一个研究人群有限的单中心研究。仍需要一个多机构的研究项目来获得更多的证据。
本期中文内容
苏雅惠
/初稿
李逸尘
/初审
范成铭
/校审
范成铭,博士
The Thoracic and Cardiovascular Surgeon 编委
中南大学湘雅二医院
外科学博士,药学博士后,副研究员,博士研究生导师,中南大学湘雅二医院心血管外科主治医师,中华志愿者协会中西医结合专家志愿者委员会心外科专业组常务委员,中国研究型医院学会心脏瓣膜病专业委员会青年委员,湖南省医学会胸心血管外科学专业委员会青年委员,美国阿拉巴马大学伯明翰分校生物医学工程学系国家公派联合培养博士,中南大学十佳大学生、中南大学湘雅二医院青年岗位能手、十佳青年、湖南省卫生健康高层次人才,中南大学“升华学者计划”优秀青年人才。美国胸外科协会(AATS) Evarts A. Graham Memorial Traveling Fellowship 2023年获得者(首位获得该奖项的国内心外科医生,每年仅资助一名心外科医师)。美国Samuel and Jean Frankel心血管中心Fellow。荷兰Catharina医院心胸外科Fellow,比利时Cliniques universitaires Saint-Luc医院心胸血管外科Fellow。主持国家自然科学基金2项、湖南省优秀青年科研基金、湖南省优秀博士后基金各1项,先后获省优秀博士研究生学位论文奖、湖南省医学科技一等奖2项,科技进步二等奖1项,医学十大临床创新技术奖1项。主要研究方向为缺血性心脏病的细胞相关治疗研究,以第一或通讯作者身份在国内外学术期刊发表学术论文30余篇,现担任SCI期刊:Journal of the Renin-Angiotensin-Aldosterone System主编、Clinical and Experimental Hypertension主编,Journal of Cardiothoracic Surgery、BMC Bioinformatics副主编,Clinical Case Reports高级主编,European Journal of Medical Research副主编及心脏病学栏目主编,BioMed Research International、PLoS ONE、PeerJ学术主编,BMC Medicine、Reviews in Cardiovascular Medicine、Thoracic and Cardiovascular Surgeon、BMC Cardiovascular Disorders等多本SCI杂志编委。
德国胸心血管外科学会会刊。
The Thoracic and Cardiovascular Surgeon 发表来自国际公认的胸心血管外科医师、心脏病学家、麻醉学家、生理学家和病理学家的最高标准文章。本刊是这一领域工作者的重要资源。
原创论文、简讯、综述和重要会议公告将报告关键的临床进展,同时为读者提供心血管和胸外科的理论背景。病例报告在我们的开放获取姊妹期刊The Thoracic and Cardiovascular Surgeon Reports上发表。
