

科学的未来只能属于勤奋而谦虚的年轻一代!
— 巴甫洛夫 —
/
本文作者:那些年的阿司匹林
北京天坛医院神经外科专硕在读。在一个温馨、实力雄厚的科研团队,从一名科研小白慢慢成长起来。目前SCI已发3篇(影响因子最高4.0),在投3篇(影响因子最高5.6),4项专利在申请,已授权2项。
本文作者独家授权,转载请注明。
//
如何完成第一篇基础实验设计
特别喜欢金庸老先生的《笑傲江湖》,里面有这么一段介绍剑宗与气宗之争的:剑宗功夫易于速成,见效极快。大家都练十年,定是剑宗占上风;各练二十年,那是各擅胜场,难分上下;要到二十年之后,练气宗功夫的才渐渐的越来越强;到得三十年时,练剑宗功夫的便再也不能望气宗之项背了。
修炼科研同样也是如此,关于气宗的修炼在于平时的日积月累,注重修炼独特的科研思维,再深下几年苦功夫,还得有充足的科研经费支持,这是大佬们所考虑的。当然,想成为自己领域的台柱子,气宗的修炼必不可少。但对于我们这些科研小白来说,就喜欢短平快,也就是所谓的套路, 接下来我将详细介绍如何完成自己的第一篇SCI。
首先从实验设计开始。
这里所介绍的经验都是笔者亲身经历,但是换个基因、换个瘤子,套路还是会一样有效。所以科研方法还是可以借鉴的。
接上篇介绍肿瘤的侵袭特性(还没读过的同学,请点击这里穿越),那么我们就先从肿瘤侵袭入手吧。
了解到要研究肿瘤侵袭的特性之后,我们便想了解目前前沿的研究关于垂体瘤做到哪了,还有哪些基因是我们没有做到的。首先在PubMed上检索文献,初步筛查后挑选几篇综述看看,学习综述是你了解这个领域内的知识最便捷有效的方式,因为它涵括了近几年该领域的汇总信息。笔者挑选学习了几篇文献后大致心里有初步的了解,见下图[1]。
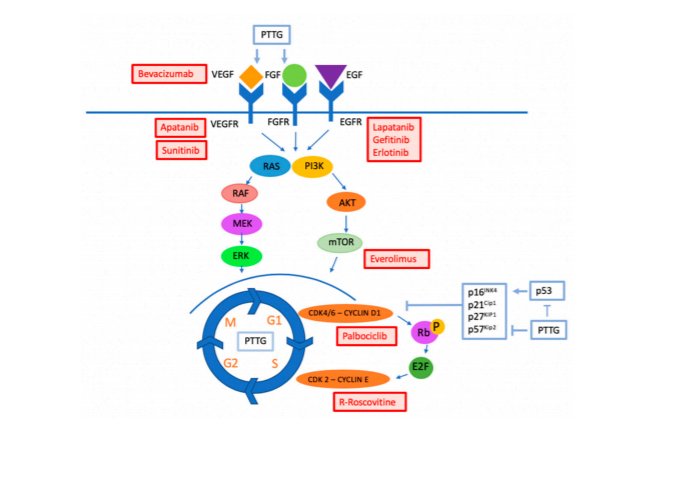
这幅图基本涵括了目前垂体瘤发生发展的研究机制,而且是确定的,我们大致可以发现有这么几条主线:
1.生长因子及受体:血管内皮生长因子(VEGF);表皮生长因子受体(epidermal growth factor receptor, EGFR);纤维母细胞生长因子(FGF)及其受体;
2.信号通路:PI3K/Akt/mTOR和Raf/Mek/ERK通路;Notch和Hedgehog信号通路;
3.细胞周期;
4.肿瘤免疫(文末有具体的影响作用机制说明)。
前人的研究就是我们研究的基础,之所以我们可以走的又快又远就是因为可以站在前人的肩膀上,基于此,无论从什么基因或者因子出发,最可靠的方式终究要落实到以上所涉猎的通路或因子或周期上来。
跟老板讨论后建议我做周期蛋白,因为肿瘤的复发或者增殖,抑或侵袭迁移能力的增加都是细胞异常分裂进而导致生物特性的改变,因此,细胞周期值得尝试。现有的影响垂体瘤的周期蛋白肯定不能再做了,于是选择了另外几个,同样检索文献,发现在胶质瘤以及肺癌、膀胱癌、肝癌等都有相应的细胞周期蛋白的异常表达,因此综合meta分析的结果挑选了几个候选的周期蛋白基因。接下来就是进行验证,看哪个周期蛋白基因对侵袭性垂体瘤的影响最明显,这个可以通过PCR及Western Blot来验证。挑选差异最明显的周期蛋白基因作为研究的分子。
接下来要设计相应的功能试验验证,这要在细胞中进行,单基因功能试验的验证简单的就是基因的敲减或者过表达,然后看表型的变化。简单而言,如果该基因在侵袭性肿瘤中高表达,那么建议做基因的敲减;如果低表达,建议做基因的过表达。当然精力允许的话都做是最好的了。这些都可以通过相应的细胞生物学方法来实现,在接下来的更新中会详细介绍。干扰完基因之后,进行表型验证,比如通过CCK-8检测细胞活力,克隆形成实验检测细胞增殖,流式检测细胞凋亡,Transwell实验检测细胞侵袭迁移能力等等。
现在,只是表型说明这个基因影响功能,要想发高分,提升文章档次,还要涉及机制研究。
既然研究的是肿瘤侵袭迁移的特性,就要考虑到导致侵袭迁移发生的机制。目前权威的假说即EMT(上皮-间质转化)。
EMT指上皮细胞失去其细胞极性和细胞-细胞粘附,并获得迁移和侵袭特性而成为间充质干细胞的过程[2]。影响EMT的指示蛋白主要有N-cadherin及E-cadherin。所以,接下来就要验证周期蛋白与EMT指标之间的调控关系。
首先从组织学水平,高侵袭的肿瘤与非侵袭肿瘤对比N-cadherin及E-cadherin的表达水平,以及与周期蛋白基因的相关性,可以通过RT-PCR及Western Blot实现。进而呢在细胞水平,干扰完细胞周期蛋白基因后检测N-cadherin及E-cadherin的表达。最后是动物实验,在细胞水平干扰细胞周期蛋白基因,然后将细胞移植到裸鼠皮下进行成瘤实验(具体实验操作后续更新),成瘤过程中观察肿瘤大小及重量变化,最后取出肿瘤,检测移植瘤中细胞周期蛋白及N-cadherin及E-cadherin的表达,这个可以做WB或者免疫组化。这样我们就完成了从组织—细胞—动物的整个实验设计。
以上是整个实验的思路,看起来简单,但是每一步都有许多未知不确定的情况发生,就比如选择研究的目的基因,可能分析来分析去,筛来筛去,最后一验证发现并不表达或者表达并没有什么差异,差异不大的话后期的实验将会很难做,所以实力很关键,有时候运气也挺重要的。这就相当于顺着一棵大树的枝枝蔓蔓去找主干,很多人最终找到的就可能是某一条小的分枝,对整体的影响微乎其微。所以,修炼科研,也要修炼平常心,耐得住寂寞,坐得了冷板凳,才能有正果。其实,整个实验设计还是走了不少的弯路,每遇到一个瓶颈,能解决就想办法解决,解决不了就换个思维方式去试试,这也是试过了几次才找到的路。
接下来,将会进行实验具体的操作及注意事项的介绍。文章构思机制图,如下:
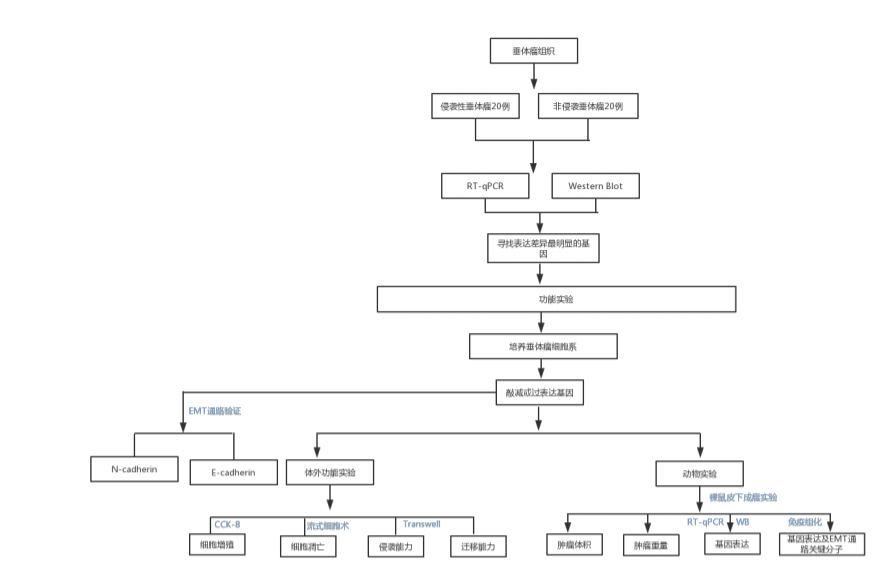
///
补充说明
1.血管内皮生长因子(VEGF),促进血管生成和血管通透性,调节肿瘤免疫微环境,在肿瘤发生中起关键作用;
2. 表皮生长因子受体(epidermal growth factor receptor, EGFR)可促进细胞增殖、抑制凋亡的膜受体酪氨酸激酶,促进细胞增殖、抑制凋亡的膜受体酪氨酸激酶。
3. 纤维母细胞生长因子(FGF)及其受体参与细胞增殖、存活、迁移和分化的调控,在血管生成中发挥重要作用。FGF信号的失调通过驱动细胞增殖有助于肿瘤发生和促进血管生成。
4. PI3K/Akt/mTOR和Raf/Mek/ERK通路:调节细胞周期增殖和分化、细胞生存、蛋白质合成、和细胞代谢,
5.Notch和Hedgehog信号通路:Notch信号通路调控正常细胞的增殖和分化,与癌症生物学相关,影响包括肿瘤干细胞、免疫细胞、内皮细胞和肿瘤细胞等多种肿瘤细胞类型。Hedgehog信号通路参与干细胞的维持和内稳态(maintenance and homeostasis),调节细胞增殖、存活和血管生成。

参考文献:
1. LS L, HW S, AI M. Exploring the Role of Novel Medical Therapies for Aggressive Pituitary Tumors: A Review of the Literature-"Are We There Yet?". Cancers. 2020; 12.
2. J Y, P A, G B, C B, T B, M B, K C, A C, J C, G C, S D, R D, HL F, et al. Guidelines and definitions for research on epithelial-mesenchymal transition. Nature reviews Molecular cell biology. 2020; 21: 341-52.
- end -
